kategória: Najlepšie články » Začiatočníci elektrikári
Počet zobrazení: 36288
Komentáre k článku: 1
Zdroje chemického prúdu: hlavné charakteristiky
 Viac ako dve storočia ľudstvo využíva energiu chemických reakcií medzi rôznymi látkami na výrobu jednosmerného prúdu.
Viac ako dve storočia ľudstvo využíva energiu chemických reakcií medzi rôznymi látkami na výrobu jednosmerného prúdu.
Pracovný princíp
Redoxná reakcia, ku ktorej dochádza medzi látkami s vlastnosťami oxidačného činidla a redukčného činidla, je sprevádzaná uvoľňovaním elektrónov, ktorých pohyb vytvára elektrický prúd. Aby sa však využila jeho energia, je potrebné vytvoriť podmienky na priechod elektrónov vonkajším obvodom, inak sa uvoľňuje teplom z jednoduchej zmesi oxidačného činidla a redukčného činidla.
Preto všetky zdroje chemického prúdu majú dve elektródy:
-
anóda, pri ktorej dochádza k oxidácii;
-
katóda, uskutočňujúca obnove látky.
Elektródy na diaľku sú umiestnené v nádobe s elektrolytom - látkou, ktorá vedie v dôsledku procesov disociácie média na ióny elektrický prúd.
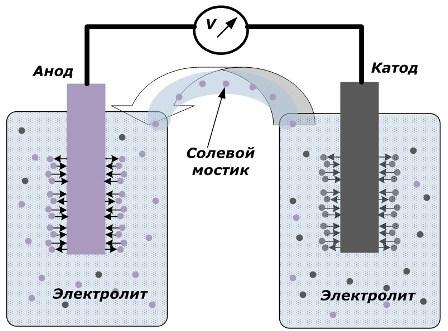
Princíp premeny chemickej energie na elektrickú energiu
Obrázok ukazuje, že elektródy sú umiestnené v samostatných nádobách spojených soľným mostíkom, ktorým sa vytvára pohyb iónov pozdĺž vnútorného obvodu. Ak sú vonkajšie a vnútorné obvody otvorené, na elektródach nastanú dva procesy: prechod iónov z kovu elektródy na elektrolyt a prechod iónov z elektrolytu do kryštálovej mriežky elektród.
Prietoky týchto procesov sú rovnaké a na každej elektróde sa akumuluje napäťový potenciál opačných znakov. Ak sú prepojené cez soľný most a pôsobí záťaž, dôjde k vytvoreniu elektrického obvodu. Vnútorný prúd je generovaný pohybom iónov medzi elektródami cez elektrolyt a soľný mostík. Pohyb elektrónov pozdĺž vonkajšieho obvodu v smere od anódy k katóde.
Takmer všetky redoxné reakcie sú sprevádzané výrobou elektriny. Jeho hodnota však závisí od mnohých faktorov, vrátane objemu a hmotnosti použitých chemikálií, materiálov použitých na výrobu elektród, ako je elektrolyt, koncentrácia iónov, návrh.
Najbežnejšie používané v moderných chemických zdrojoch sú:
-
pre materiál anódy (redukčné činidlo), zinku (Zn), olova (Pb), kadmia (Cd) a niektorých ďalších kovov;
-
pre katódový materiál (oxidačné činidlo) - oxid olovnatý PbO2, oxid manganičitý MnO2, hydroxid nikelnatý NiOOH a ďalšie;
-
elektrolyty na báze roztokov kyselín, zásad alebo solí.
Klasifikačné metódy
Jedna časť zdrojov chemickej energie sa môže opätovne použiť, zatiaľ čo druhá nie. Táto zásada sa považuje za základ pre ich klasifikáciu.
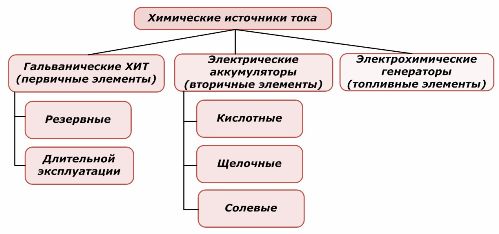
Klasifikácia chemických prvkov
Elektromotorická sila galvanické články, v závislosti od konštrukcie, dosahuje 1,2 ÷ 1,5 voltu. Aby sa získali veľké hodnoty, kombinujú sa do batérií a sériovo sa pripájajú. Ak sú batérie pripojené paralelne, zvyšuje sa prúd a energia.
Všeobecne sa uznáva, že zdroje primárneho chemického prúdu nepodporujú nabíjanie, hoci presnejšie je možné túto pozíciu formulovať odlišne: jej vykonávanie nie je ekonomicky uskutočniteľné.
Redundantné zdroje primárneho chemického prúdu sú uložené v stave, v ktorom je elektrolyt izolovaný od elektród. To eliminuje výskyt redoxnej reakcie a zabezpečuje pripravenosť na uvedenie do prevádzky. Nie sú znovu použité. Skladovateľnosť chemických záložných zdrojov energie je obmedzená na 10–15 rokov.
Batérie sa úspešne nabíjajú pôsobením vonkajšej elektrickej energie. Vďaka tejto vlastnosti sa nazývajú sekundárne zdroje prúdu. Sú schopné vydržať stovky a tisíce cyklov vybíjania a vybíjania.EMF batérie môže byť v rozsahu 1,0 ÷ 1,5 V. Sú tiež kombinované do batérií.
Elektrochemické generátory pracujú na princípe galvanických článkov, ale pri vykonávaní elektrochemickej reakcie látky prichádzajú zvonka a všetky uvoľňované produkty sa z elektrolytu odstránia. To vám umožní zorganizovať nepretržitý proces.
Kľúčové vlastnosti chemických zdrojov energie
1. Napätie na otvorených svorkách
V závislosti od dizajnu môže jediný zdroj vytvoriť iba určitý potenciálny rozdiel. Na použitie v elektrických zariadeniach sa kombinujú do batérií.
2. Špecifická kapacita
Jeden zdroj chemického prúdu môže určitý čas (v hodinách) generovať obmedzené množstvo prúdu (v ampéroch), ktoré sa pripisuje jednotke hmotnosti alebo objemu.
3. Výkonová hustota
Charakterizuje schopnosť jednotky hmotnosti alebo objemu zdroja chemického prúdu generovať energiu generovanú produktom napätia podľa sily prúdu.
4. Trvanie činnosti
Tento parameter sa nazýva aj dátum exspirácie.
5. Hodnota samovybíjacích prúdov
Tieto vedľajšie procesy elektrochemických reakcií vedú k spotrebe aktívnej hmoty prvkov, spôsobujú koróziu a znižujú špecifickú kapacitu.
6. Cena produktu
Závisí od konštrukcie, použitých materiálov a radu ďalších faktorov.
Najlepšie zdroje chemického prúdu sú zdroje s vysokými hodnotami prvých štyroch parametrov a samovybíjanie a náklady sú nízke.
Zásady nabíjania batérie
Medzi sekundárnymi chemickými zdrojmi získavajú veľkú obľubu. lítium-iónové modely, ktoré sa bežne používajú na napájanie elektronických zariadení. Ako materiál kladnej elektródy používajú LiMO2 (M Co, Ni, Mn) a ako negatív grafit.
Po nabití sú lítiové ióny z aplikovanej vonkajšej energie uvoľňované z katódového kovu, prechádzajú elektrolytom a prenikajú do priestoru medzi grafitovými vrstvami, kde sa akumulujú.
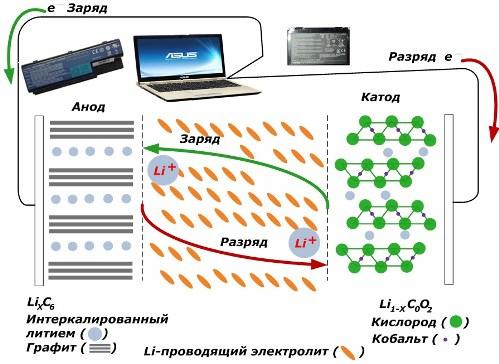
Keď je energia nabíjačka "Chýba" a záťaž je spojená s elektródami, potom sa lítne ióny v elektrolyte pohybujú v opačnom smere.
Ak sa nabíjanie a vybíjanie nevykoná, energia v batérii sa nespotrebuje, ale uloží. Jeho množstvo je však obmedzené vlastnosťami použitých materiálov. Napríklad v lítium-iónových batériách je špecifická elektrická kapacita 130 ÷ 150 mAh / g. Je obmedzená vlastnosťami anódového materiálu. V prípade grafitu je kapacita asi dvakrát vyššia.
Vedci teraz hľadajú spôsoby, ako zvýšiť kapacitu batérie, skúmajú možnosť použitia chemickej reakcie medzi lítiom a kyslíkom vo vzduchu. Na tento účel sa vyvíjajú dizajny so vzduchovou, nespotrebiteľnou katódou, ktorá sa používa v samostatných batériách. Táto metóda môže zvýšiť hustotu energie až 10-krát.
Prevádzka chemických zdrojov prúdu si vyžaduje znalosti základy elektrotechniky, elektrochémia, veda o materiáloch a fyzika tuhých látok.
Pozri tiež na bgv.electricianexp.com
:
