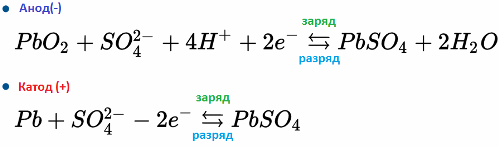kategória: Ako to funguje, Auto elektrikár
Počet zobrazení: 16526
Komentáre k článku: 0
Prístroj a princíp činnosti batérie
Elektrická batéria sa volá opakovane použiteľný zdroj chemického prúdu, Chemické procesy vo vnútri batérie, na rozdiel od procesov v jednorazových galvanických článkoch, ako sú alkalické alebo soľné batérie, sú reverzibilné. Cykly vybíjania, akumulácie a návratu elektrickej energie sa môžu mnohokrát opakovať.
Princíp činnosti batérie vám teda umožňuje cyklicky ju používať na autonómne napájanie rôznych zariadení, prenosných zariadení, vozidiel, lekárskeho vybavenia atď. V úplne odlišných oblastiach.

Keď sa hovorí slovo „batéria“, znamená to buď samotnú batériu, alebo batériu. Batériu tvorí niekoľko sériových alebo paralelne prepojených batérií, ako aj niekoľko pripojených batérií.
Prvá batéria, čiže opakovane použiteľná galvanická bunka, sa podľa oficiálnych údajov objavila v roku 1803. Vytvoril ho nemecký fyzik a chemik Johann Wilhelm Ritter. Priateľ Oersted, Ritter, ktorý nie je vedcom, študoval chemický účinok svetla, experimentoval s elektrolýzou, mimochodom, patrí k objavu ultrafialovej časti elektromagnetického spektra.
Pri experimentovaní s voltaickým stĺpcom vzal Ritter päťdesiat kruhov medi, kúsky vlhkej látky a vytvoril stĺpec z päťdesiatich takýchto kruhov a vlhkej látky medzi nimi. Ritter, ktorý prešiel prúdom z voltaického stĺpca cez štruktúru, zistil, že jeho pól bol nabitý a sám sa stal zdrojom elektriny. Bola to prvá batéria.
Reverzibilita chemickej reakcie v elektrolyte a na elektródach batérie vám umožňuje obnoviť účinnosť batérie - nabiť ju po vybití. Prúd počas nabíjania prechádza batériou v opačnom smere ako je výboj.
Napríklad olovená batéria pracuje v dôsledku elektrochemických reakcií olova a oxidu olovnatého v kyseline sírovej. Vzorce uvedené nižšie odrážajú reverzibilné reakcie vyskytujúce sa na anóde a na katóde: zľava doprava - reakcia počas vybíjania, sprava doľava.
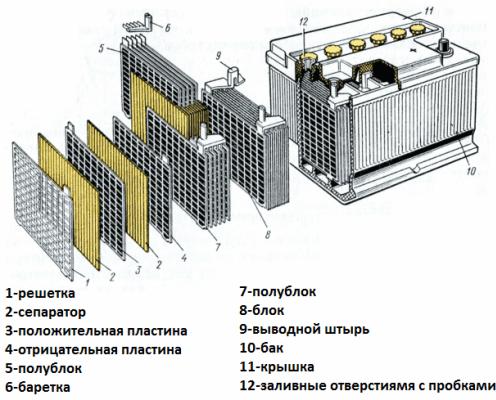
Teraz zvážte batériové zariadenie ako príklad štartovacej batérie do auta. Jeho napätie je 12 voltov. Batéria sa skladá zo šiestich článkov zapojených do série, oddelených priečkami.
Sériové pripojenie v tomto prípade znamená, že záporný terminál jednej bunky je pripojený k pozitívnemu terminálu nasledujúcej bunky.
Každý prvok obsahuje pár mriežkových elektród zliatiny olova a antimónu ponorených do elektrolytu, čo je 38% vodný roztok kyseliny sírovej. Porézny oddeľovač izoluje elektródy od seba, čím bráni skratom medzi nimi, ale voľne prechádza elektrolyt cez seba. To znamená, že kvapalina vyplňuje bunky olovených platní aj póry separátorov.
Dosky s rovnakým názvom sú vzájomne prepojené olovnatými prepojkami, ako aj balíky dosiek oddelené priečkami, ktoré tvoria jednotlivé prvky, a svorky batérie sú tiež vyrobené z olova.
Závery autobatérie sú vždy navzájom mierne odlišné - kladný terminál má väčší priemer ako záporný, aby nedošlo k chybe pri pripojení.
Puzdro na batériu je vyrobené z dielektrického materiálu odolného voči agresívnemu prostrediu, extrémnym teplotám a vibráciám. Dnes sú štartovacie puzdrá batérií vyrobené z polypropylénu.
Puzdro je hermeticky uzavretý kontajner s vekom, vybavený prírubami pre trvalú montáž.V puzdrách starých batérií boli vždy umiestnené zátky pre každý galvanický článok tvoriaci batériu, takže v prípade potreby bolo možné pridať destilovanú vodu. Moderné bezúdržbové zástrčky batérií na skriniach nemajú.
Ďalšie články o batériách a ich použití:
Ako sa majú batérie pre solárne elektrárne
Pozri tiež na bgv.electricianexp.com
: